ISO 11135 是针对环氧乙烷(EO)灭菌过程的国际标准,旨在通过规范灭菌流程,确保医疗器械达到预设的无菌保证水平(SAL,通常为 10⁻⁶),适用于对热、湿敏感的医疗器械。
适用的产品:怕热、怕湿的器械,比如塑料输液管、电子医疗设备。
关键点:控制 EO 浓度、温度、灭菌时间,还要严格检测灭菌后残留的 EO(有毒性,需达标)。
ISO 11137 针对辐射灭菌过程(包括 γ 射线、电子束、X 射线),规范通过电离辐射杀灭微生物的流程,适用于耐辐射的医疗器械。
适合产品:耐辐射、耐高温的器械,比如金属手术刀、一次性注射器。
关键点:确定合适的辐射剂量(既要杀死细菌,又不损坏产品),监控剂量均匀性,无化学残留。
必备条件:
ISO 11135(环氧乙烷灭菌):
1.产品能扛住 EO 气体和灭菌环境(温湿度),且 EO 残留量达标(无毒)。
2.严格控 EO 浓度、温度、时间,确保参数稳定。
3.用生物指示剂验证灭菌效果,达到 “100 万个产品最多 1 个有菌” 的安全标准。
4.灭菌后充分通风除残留,操作人员做好防护。
ISO 11137(辐射灭菌):
1.产品耐辐射,不会因辐射变脆、失效。
2.确定合适辐射剂量(既要杀完菌,又不损坏产品),且剂量在产品上分布均匀。
3.用剂量计实时监控辐射量,确保符合设定值。
4.验证不同批次、装载方式下灭菌效果一致,达到上述安全标准。
资料清单:
ISO 11135(环氧乙烷灭菌):
产品相关文件;质量管理体系文件;灭菌过程验证资料;残留控制资料;安全与追溯资料;
ISO 11137(辐射灭菌):
产品相关文件;质量管理体系文件;剂量设定与验证资料;辐射过程监控资料;产品稳定性资料;
服务流程:
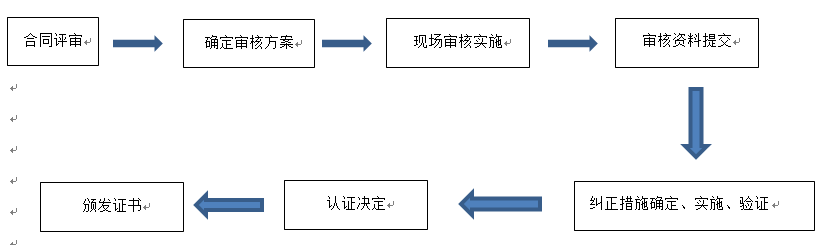
预计完成时间:
若企业资料完整、验证充分,且审核无重大问题,最快可 3 个月内完成;若存在多次整改或补测,时间可能延长至 6 个月以上。